Brand Temovate 15g Clobetasol Uso, Effetti Collaterali e Dosaggio. Prezzo in farmacia online. Farmaci generici senza ricetta.
Cos'è Temovate e come si usa?
Temovate è un medicinale soggetto a prescrizione medica usato per trattare i sintomi della psoriasi a placche e del cuoio capelluto e le dermatosi sensibili ai corticosteroidi. Temovate può essere usato da solo o con altri farmaci.
Temovate appartiene a una classe di farmaci chiamati corticosteroidi, topici.
Non è noto se Temovate sia sicuro ed efficace nei bambini di età inferiore ai 12 anni.
Quali sono i possibili effetti collaterali di Temovate?
Temovate può causare gravi effetti collaterali tra cui:
- peggioramento delle condizioni della tua pelle,
- arrossamento, calore, gonfiore, stillicidio o grave irritazione della pelle trattata,
- visione offuscata,
- visione a tunnel,
- dolore all'occhio,
- vedendo aloni intorno alle luci,
- aumento della sete,
- bocca asciutta,
- odore di alito fruttato,
- aumento di peso sul viso e sulle spalle,
- lenta guarigione delle ferite,
- scolorimento della pelle,
- pelle assottigliata,
- aumento dei peli sul corpo,
- stanchezza,
- cambiamenti di umore,
- cambiamenti mestruali, e
- cambiamenti sessuali
Chiedi immediatamente assistenza medica, se hai uno dei sintomi sopra elencati.
Gli effetti collaterali più comuni di Temovate includono:
- bruciore, prurito, gonfiore o irritazione della pelle trattata,
- pelle secca o screpolata,
- arrossamento o formazione di croste intorno ai follicoli piliferi,
- vene a ragnatela,
- smagliature,
- pelle assottigliata,
- eruzione cutanea o orticaria,
- acne, e
- caduta temporanea dei capelli
Informi il medico se ha qualche effetto collaterale che ti infastidisce o che non scompare.
Questi non sono tutti i possibili effetti collaterali di Temovate. Per ulteriori informazioni, chiedi al tuo medico o al farmacista.
Chiamate il vostro medico per un consiglio medico circa gli effetti collaterali. È possibile segnalare gli effetti collaterali alla FDA al numero 1-800-FDA-1088.
DESCRIZIONE
TEMOVATE® (crema e unguento a base di clobetasolo propionato) Crema e unguento, contiene lo 0,05% del composto attivo clobetasolo propionato, un corticosteroide sintetico, per uso dermatologico topico. Clobetasol, un analogo del prednisolone, ha un alto grado di attività glucocorticoide e un leggero grado di attività mineralcorticoide.
Chimicamente, il clobetasolo propionato è (11ß,16ß)-21-cloro-9-fluoro-11-idrossi-16-metil-17-(1-ossopropossi)-pregna-1,4-diene-3,20-dione e ha la seguente formula strutturale:
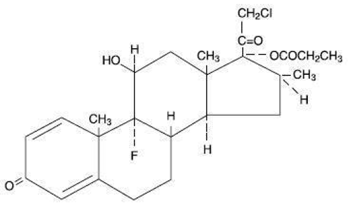
Il clobetasolo propionato ha la formula molecolare C25H32CIFO5 e un peso molecolare di 467. È una polvere cristallina di colore da bianco a crema insolubile in acqua.
TEMOVATE® Crema contiene clobetasolo propionato 0,5 mg/g in una crema a base di glicole propilenico, gliceril monostearato, alcool cetostearilico, gliceril stearato, PEG 100 stearato, cera bianca, clorocresolo, sodio citrato, acido citrico monoidrato e acqua purificata.
TEMOVATE® Unguento contiene clobetasolo propionato 0,5 mg/g in una base di glicole propilenico, sorbitano sesquioleato e vaselina bianca.
INDICAZIONI
TEMOVATE® Crema e Unguento sono formulazioni corticosteroidi ad altissima potenza indicate per il sollievo delle manifestazioni infiammatorie e pruriginose delle dermatosi responsive ai corticosteroidi. Il trattamento oltre le 2 settimane consecutive non è raccomandato e il dosaggio totale non deve superare i 50 g/settimana a causa della potenziale soppressione dell'asse ipotalamo-ipofisi-surrene (HPA) del farmaco. L'uso in pazienti pediatrici di età inferiore a 12 anni non è raccomandato.
Come con altri corticosteroidi altamente attivi, la terapia deve essere interrotta quando il controllo è stato raggiunto. Se non si osserva alcun miglioramento entro 2 settimane, potrebbe essere necessaria una rivalutazione della diagnosi.
DOSAGGIO E SOMMINISTRAZIONE
Applicare uno strato sottile di TEMOVATE® Crema o Unguento sulle zone cutanee interessate due volte al giorno e massaggiare delicatamente e completamente (vedi INDICAZIONI E UTILIZZO ).
La crema e l'unguento TEMOVATE® sono corticosteroidi topici ad altissima potenza; dunque, il trattamento deve essere limitato a 2 settimane consecutive e non devono essere utilizzate quantità superiori a 50 g/settimana.
Come con altri corticosteroidi altamente attivi, la terapia deve essere interrotta quando il controllo è stato raggiunto. Se non si osserva alcun miglioramento entro 2 settimane, può essere necessaria una rivalutazione della diagnosi.
TEMOVATE® Cream and Unguento non deve essere utilizzato con medicazioni occlusive.
Uso geriatrico
Negli studi in cui i pazienti geriatrici (di età pari o superiore a 65 anni, cfr PRECAUZIONI sono stati trattati con TEMOVATE® Crema o Pomata, la sicurezza non differiva da quella dei pazienti più giovani; pertanto, non è raccomandato alcun aggiustamento del dosaggio.
COME FORNITO
TEMOVATE® (crema di clobetasolo propionato) Crema, 0,05% è fornito in:
Tubi da 30 g ( NDC 10337-163-30) e provette da 60 g ( NDC 10337-163-60).
TEMOVATE® (unguento al propionato di clobetasolo) Unguento, lo 0,05% è fornito in:
Tubi da 15 g ( NDC 10337-162-15) e provette da 30 g ( NDC 10337-162-30).
Conservare tra 15° e 30°C (59° e 86°F). TEMOVATE® Cream non deve essere refrigerata. PharmaDerm
Una divisione di Fougera Pharmaceuticals Inc., Melville, NY 11747 USA. Revisionato: gennaio 2012
EFFETTI COLLATERALI
Negli studi clinici controllati, le reazioni avverse più frequenti riportate per TEMOVATE® Cream sono state sensazione di bruciore e bruciore nell'1% dei pazienti trattati. Reazioni avverse meno frequenti sono state prurito, atrofia cutanea e screpolature e screpolature della pelle.
Negli studi clinici controllati, gli eventi avversi più frequenti riportati per TEMOVATE® Unguento sono stati sensazione di bruciore, irritazione e prurito nello 0,5% dei pazienti trattati. Reazioni avverse meno frequenti sono state bruciore, screpolature, eritema, follicolite, intorpidimento delle dita, atrofia cutanea e teleangiectasia.
La sindrome di Cushing è stata segnalata nei neonati e negli adulti a seguito dell'uso prolungato di formulazioni topiche di clobetasolo propionato.
Le seguenti reazioni avverse locali aggiuntive sono state riportate con i corticosteroidi topici e possono verificarsi più frequentemente con l'uso di medicazioni occlusive e corticosteroidi di maggiore potenza. Queste reazioni sono elencate in ordine di insorgenza approssimativamente decrescente: secchezza, eruzioni acneiformi, ipopigmentazione, dermatite periorale, dermatite allergica da contatto, infezione secondaria, irritazione, strie e miliaria.

INTERAZIONI DI DROGA
Nessuna informazione fornita.
AVVERTENZE
Nessuna informazione fornita. Perfavore guarda PRECAZIONI sezione sottostante.
PRECAUZIONI
Generale
TEMOVATE® Crema e Unguento non deve essere utilizzato nel trattamento della rosacea o della dermatite periorale e non deve essere utilizzato su viso, inguine o ascelle.
L'assorbimento sistemico dei corticosteroidi topici può produrre una soppressione reversibile dell'asse HPA con il potenziale di insufficienza di glucocorticosteroidi dopo la sospensione del trattamento. Manifestazioni di sindrome di Cushing, iperglicemia e glicosuria possono anche essere prodotte in alcuni pazienti dall'assorbimento sistemico di corticosteroidi topici durante la terapia.
I pazienti che applicano uno steroide topico su un'ampia superficie o su aree sotto occlusione devono essere valutati periodicamente per l'evidenza della soppressione dell'asse HPA. Questo può essere fatto utilizzando la stimolazione con ACTH, il cortisolo plasmatico AM e i test del cortisolo libero urinario. I pazienti che ricevono corticosteroidi superpotenti non devono essere trattati per più di 2 settimane alla volta e solo piccole aree devono essere trattate alla volta a causa dell'aumentato rischio di soppressione dell'HPA.
TEMOVATE® Cream and Unguento ha prodotto la soppressione dell'asse HPA quando utilizzato a dosi fino a 2 g/die per 1 settimana in pazienti con eczema.
Se si nota la soppressione dell'asse HPA, si dovrebbe tentare di sospendere il farmaco, di ridurre la frequenza di applicazione o di sostituire un corticosteroide meno potente. Il recupero della funzione dell'asse HPA è generalmente rapido dopo l'interruzione dei corticosteroidi topici. Raramente possono verificarsi segni e sintomi di insufficienza di glucocorticosteroidi che richiedono corticosteroidi sistemici supplementari. Per informazioni sulla supplementazione sistemica, vedere le informazioni sulla prescrizione di tali prodotti.
I pazienti pediatrici possono essere più suscettibili alla tossicità sistemica da dosi equivalenti a causa della loro maggiore superficie cutanea in rapporto alla massa corporea (vedi PRECAUZIONI : Uso pediatrico ).
Se si sviluppa irritazione, sospendere TEMOVATE® Crema e Pomata e istituire una terapia appropriata. La dermatite allergica da contatto con corticosteroidi viene solitamente diagnosticata osservando una mancata guarigione piuttosto che notando un'esacerbazione clinica come con la maggior parte dei prodotti topici non contenenti corticosteroidi. Tale osservazione dovrebbe essere corroborata da appropriati patch test diagnostici.
Se sono presenti o si sviluppano infezioni cutanee concomitanti, deve essere utilizzato un agente antimicotico o antibatterico appropriato. Se una risposta favorevole non si verifica tempestivamente, l'uso di TEMOVATE® Crema e Unguento deve essere interrotto fino a quando l'infezione non è stata adeguatamente controllata.
Test di laboratorio
I seguenti test possono essere utili per valutare i pazienti per la soppressione dell'asse HPA:
Test di stimolazione con ACTH Test del cortisolo plasmatico AM Test del cortisolo libero urinario
Cancerogenesi, mutagenesi, compromissione della fertilità
Non sono stati condotti studi a lungo termine sugli animali per valutare il potenziale cancerogeno del clobetasolo propionato.
Studi nel ratto dopo somministrazione sottocutanea a livelli di dosaggio fino a 50 mcg/kg/die hanno rivelato che le femmine hanno mostrato un aumento del numero di embrioni riassorbiti e una diminuzione del numero di feti vivi alla dose più alta.
Il clobetasolo propionato non è risultato mutageno in 3 diversi sistemi di test: il test di Ames, il test di conversione genica del Saccharomyces cerevisiae e il test di fluttuazione di E. coli B WP2.
Gravidanza
Effetti teratogeni
Gravidanza Categoria C. È stato dimostrato che i corticosteroidi sono teratogeni negli animali da laboratorio quando somministrati per via sistemica a livelli di dosaggio relativamente bassi. Alcuni corticosteroidi-teroidi hanno dimostrato di essere teratogeni dopo l'applicazione cutanea ad animali da laboratorio.
Il clobetasolo propionato non è stato testato per la teratogenicità se applicato localmente; tuttavia, viene assorbito per via percutanea e, quando somministrato per via sottocutanea, è stato un teratogeno significativo sia nel coniglio che nel topo. Il clobetasolo propionato ha un potenziale teratogeno maggiore rispetto agli steroidi meno potenti.
Gli studi di teratogenicità nei topi per via sottocutanea hanno determinato fetotossicità alla dose più alta testata (1 mg/kg) e teratogenicità a tutti i livelli di dose testati fino a 0,03 mg/kg. Queste dosi sono rispettivamente circa 1,4 e 0,04 volte la dose topica umana di TEMOVATE® Crema e Unguento. Le anomalie osservate includevano palatoschisi e anomalie scheletriche.
Nei conigli, il clobetasolo propionato è risultato teratogeno a dosi di 3 e 10 mcg/kg. Queste dosi sono rispettivamente circa 0,02 e 0,05 volte la dose topica umana di TEMOVATE® Crema e Unguento. Le anomalie osservate includevano palatoschisi, cranioschisi e altre anomalie scheletriche.
Non ci sono studi adeguati e ben controllati sul potenziale teratogeno del clobetasolo propionato nelle donne in gravidanza. TEMOVATE® Crema e Unguento deve essere utilizzato durante la gravidanza solo se il potenziale beneficio giustifica il potenziale rischio per il feto.
Madri che allattano
I corticosteroidi somministrati per via sistemica compaiono nel latte materno e potrebbero sopprimere la crescita, interferire con la produzione endogena di corticosteroidi o causare altri effetti indesiderati. Non è noto se la somministrazione topica di corticosteroidi possa determinare un assorbimento sistemico sufficiente a produrre quantità rilevabili nel latte materno. Poiché molti farmaci vengono escreti nel latte materno, occorre prestare attenzione quando TEMOVATE® crema o unguento viene somministrato a una donna che allatta.
Uso pediatrico
La sicurezza e l'efficacia di TEMOVATE® Crema e Pomata nei pazienti pediatrici non sono state stabilite. L'uso in pazienti pediatrici di età inferiore a 12 anni non è raccomandato. A causa di un rapporto più elevato tra superficie cutanea e massa corporea, i pazienti pediatrici corrono un rischio maggiore rispetto agli adulti di soppressione dell'asse HPA e sindrome di Cushing quando vengono trattati con corticosteroidi topici. Sono quindi anche a maggior rischio di insufficienza surrenalica durante o dopo la sospensione del trattamento. Sono stati segnalati effetti avversi, comprese le strie, con l'uso inappropriato di corticosteroidi topici nei neonati e nei bambini.
Nei bambini trattati con corticosteroidi topici sono stati segnalati soppressione dell'asse HPA, sindrome di Cushing, ritardo della crescita lineare, aumento di peso ritardato e ipertensione endocranica. Le manifestazioni della soppressione surrenalica nei bambini includono bassi livelli di cortisolo plasmatico e un'assenza di risposta alla stimolazione con ACTH. Le manifestazioni dell'ipertensione endocranica comprendono fontanelle sporgenti, mal di testa e papilledema bilaterale.
Uso geriatrico
Un numero limitato di pazienti di età pari o superiore a 65 anni è stato trattato con TEMOVATE® Cream (n = 231) e con TEMOVATE® Unguento (n = 101) negli studi clinici statunitensi e non statunitensi. Sebbene il numero di pazienti sia troppo piccolo per consentire un'analisi separata di efficacia e sicurezza, le reazioni avverse riportate in questa popolazione sono state simili a quelle riportate dai pazienti più giovani. Sulla base dei dati disponibili, non è giustificato alcun aggiustamento del dosaggio di TEMOVATE® Crema e Unguento nei pazienti geriatrici.
OVERDOSE
TEMOVATE® Crema e Unguento applicati localmente possono essere assorbiti in quantità sufficienti per produrre effetti sistemici (vedi PRECAUZIONI ).
CONTROINDICAZIONI
TEMOVATE® (crema e unguento al propionato di clobetasolo) Crema e unguento, 0,05% sono controindicati in quei pazienti con una storia di ipersensibilità a uno qualsiasi dei componenti dei preparati.
FARMACOLOGIA CLINICA
Come altri corticosteroidi topici, il clobetasolo propionato ha proprietà antinfiammatorie, antipruriginose e vasocostrittive. Il meccanismo dell'attività antinfiammatoria degli steroidi topici, in generale, non è chiaro. Tuttavia, si ritiene che i corticosteroidi agiscano mediante l'induzione delle proteine inibitorie della fosfolipasi A2, chiamate collettivamente lipocortine. Si ipotizza che queste proteine controllino la biosintesi di potenti mediatori dell'infiammazione come le prostaglandine e i leucotrieni inibendo il rilascio del loro precursore comune, l'acido arachidonico. L'acido arachidonico viene rilasciato dai fosfolipidi di membrana dalla fosfolipasi A2.
Farmacocinetica
L'entità dell'assorbimento percutaneo dei corticosteroidi topici è determinata da molti fattori, tra cui il veicolo e l'integrità della barriera epidermica. Non è stato dimostrato che la medicazione occlusiva con idrocortisone fino a 24 ore aumenti la penetrazione; tuttavia, l'occlusione dell'idrocortisone per 96 ore migliora notevolmente la penetrazione. I corticosteroidi topici possono essere assorbiti dalla normale pelle intatta. L'infiammazione e/o altri processi patologici della pelle possono aumentare l'assorbimento percutaneo.
Gli studi eseguiti con TEMOVATE® Crema e Unguento indicano che sono nella gamma di potenza super-alta rispetto ad altri corticosteroidi topici.
INFORMAZIONI PER IL PAZIENTE
I pazienti che usano corticosteroidi topici devono ricevere le seguenti informazioni e istruzioni:
