Macrobid 50mg, 100mg Nitrofurantoin Monohydrate Uso, Effetti Collaterali e Dosaggio. Prezzo in farmacia online. Farmaci generici senza ricetta.
Cos'è Macrobid 100mg e come si usa?
Macrobid 50 mg è un medicinale su prescrizione usato per trattare i sintomi dell'infezione del tratto urinario. Macrobid 100 mg può essere utilizzato da solo o con altri farmaci.
Macrobid è un antibiotico.
Quali sono i possibili effetti collaterali di Macrobid?
Macrobid può causare gravi effetti collaterali tra cui:
- forte mal di stomaco
- diarrea acquosa o sanguinolenta
- problemi di vista
- febbre
- brividi
- tosse
- dolore al petto
- problema respiratorio
- intorpidimento, formicolio o bruciore alle mani o ai piedi
- forte dolore dietro gli occhi
- pelle pallida
- debolezza
- dolori articolari o gonfiore con febbre
- ghiandole gonfie
- dolori muscolari
- dolore, arrossamento o gonfiore alla mascella inferiore
- forte mal di testa
- ronzio nelle orecchie
- vertigini
- nausea
- dolore alla parte superiore dello stomaco (che può diffondersi alla schiena)
- vomito
- urina scura
- ingiallimento della pelle o degli occhi (ittero)
Chiedi immediatamente assistenza medica, se hai uno dei sintomi sopra elencati.
Gli effetti collaterali più comuni di Macrobid includono:
- male alla testa
- vertigini
- sonnolenza
- debolezza
- gas
- indigestione
- perdita di appetito
- nausea
- vomito
- dolori muscolari o articolari
- eruzione cutanea
- prurito
- caduta temporanea dei capelli
Informi il medico se ha qualche effetto collaterale che ti infastidisce o che non scompare.
Questi non sono tutti i possibili effetti collaterali di Macrobid. Per ulteriori informazioni, chiedi al tuo medico o al farmacista.
Chiamate il vostro medico per un consiglio medico circa gli effetti collaterali. È possibile segnalare gli effetti collaterali alla FDA al numero 1-800-FDA-1088.
Per ridurre lo sviluppo di batteri resistenti ai farmaci e mantenere l'efficacia di Macrobid 100 mg e di altri farmaci antibatterici, Macrobid deve essere usato solo per trattare o prevenire infezioni che sono provate o fortemente sospettate di essere causate da batteri.
DESCRIZIONE
La nitrofurantoina è un agente antibatterico specifico per le infezioni del tratto urinario. Il marchio Macrobid® di nitrofurantoina è un involucro di capsula di gelatina dura contenente l'equivalente di 100 mg di nitrofurantoina sotto forma di 25 mg di macrocristalli di nitrofurantoina e 75 mg di nitrofurantoina monoidrato.
Il nome chimico dei macrocristalli di nitrofurantoina è 1-[[[5-nitro-2-furanil] metilene] amino]-2,4-imidazolidinedione. La struttura chimica è la seguente:
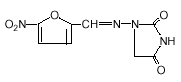 Peso Molecolare: 238,16
Peso Molecolare: 238,16 Il nome chimico della nitrofurantoina monoidrato è 1-[[[5-nitro-2-furanil] metilene] amino]-2,4-imidazolidinedione monoidrato. La struttura chimica è la seguente:
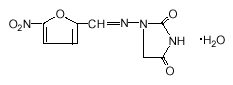 Peso Molecolare: 256,17
Peso Molecolare: 256,17 Ingredienti inattivi: ogni capsula contiene carbomer 934P, amido di mais, zucchero comprimibile, D&C Yellow n. 10, inchiostro grigio commestibile, FD&C Blue n. 1, FD&C Red n. 40, gelatina, lattosio, magnesio stearato, povidone, talco e titanio biossido.
INDICAZIONI
Macrobid è indicato solo per il trattamento delle infezioni acute non complicate del tratto urinario (cistite acuta) causate da ceppi sensibili di Escherichia coli o Staphylococcus saprophyticus.
La nitrofurantoina non è indicata per il trattamento della pielonefrite o degli ascessi perinefrici.
Per ridurre lo sviluppo di batteri resistenti ai farmaci e mantenere l'efficacia di Macrobid e di altri farmaci antibatterici, Macrobid 100 mg deve essere utilizzato solo per trattare o prevenire infezioni che sono provate o fortemente sospettate essere causate da batteri sensibili. Quando sono disponibili informazioni sulla coltura e sulla sensibilità, dovrebbero essere prese in considerazione nella selezione o nella modifica della terapia antibatterica. In assenza di tali dati, l'epidemiologia locale ei modelli di suscettibilità possono contribuire alla selezione empirica della terapia.
Le nitrofurantoine mancano della più ampia distribuzione tissutale di altri agenti terapeutici approvati per le infezioni del tratto urinario. Di conseguenza, molti pazienti trattati con Macrobid 100 mg sono predisposti alla persistenza o alla ricomparsa della batteriuria. (Vedere Studi clinici .) I campioni di urina per la coltura ei test di sensibilità devono essere ottenuti prima e dopo il completamento della terapia. Se si verifica la persistenza o la ricomparsa della batteriuria dopo il trattamento con Macrobid, devono essere selezionati altri agenti terapeutici con una distribuzione tissutale più ampia. Nel considerare l'uso di Macrobid, i tassi di eradicazione inferiori dovrebbero essere bilanciati con l'aumento del potenziale di tossicità sistemica e per lo sviluppo di resistenza antimicrobica quando vengono utilizzati agenti con una distribuzione tissutale più ampia.
DOSAGGIO E SOMMINISTRAZIONE
Le capsule di Macrobid devono essere assunte con il cibo.
Adulti e pazienti pediatrici di età superiore a 12 anni: una capsula da 100 mg ogni 12 ore per sette giorni.
COME FORNITO
Macrobid è disponibile sotto forma di capsule nere e gialle opache da 100 mg con impresso “(banda) Macrobid (banda)” su una metà e “52427-285” sull'altra.
NDC 52427-285-01 bottiglia da 100
Conservare a temperatura ambiente controllata (da 59° a 86°F o da 15° a 30°C).
Soddisfa il test di dissoluzione USP 2
RIFERIMENTI
1. Istituto per gli standard clinici e di laboratorio. Metodi per la diluizione Test di sensibilità agli antimicrobici per batteri che crescono aerobicamente; Approvato Standard-Ottava Edizione. Documento CLSI M07-A8 [ISBN 1-56238-689-1]. Clinical and Laboratory Standards Institute, 940 West Valley Road, Suite 1400, Wayne, Pennsylvania 19087- 1898 USA, 2009.
2. Istituto per gli standard clinici e di laboratorio. Standard di prestazione per i test di suscettibilità ai dischi antimicrobici; Standard approvato - Decima edizione. Documento CLSI M02-A 10 [ISBN 1-56238-688-3]. Clinical and Laboratory Standards Institute, 940 West Valley Road, Suite 1400, Wayne, Pennsylvania 19087- 1898 USA, 2009.
3. Istituto per gli standard clinici e di laboratorio. Standard di prestazione per la prova di suscettibilità antimicrobica; Supplemento informativo diciannovesimo. Documento CLSI M100-S19 [ISBN 1-56238-716-2]. Istituto per gli standard clinici e di laboratorio, 940 West Valley Road, Suite 1400, Wayne, Pennsylvania 19087-1898 USA, 2010.
Distribuito da: Almatica Pharma, Inc. Pine Brook, NJ 07058 USA. Rev: 02/2013
EFFETTI COLLATERALI
Negli studi clinici su Macrobid, gli eventi avversi clinici più frequenti segnalati come possibilmente o probabilmente correlati al farmaco sono stati nausea (8%), cefalea (6%) e flatulenza (1,5%). Ulteriori eventi avversi clinici segnalati come possibilmente o probabilmente correlati al farmaco si sono verificati in meno dell'1% dei pazienti studiati e sono elencati di seguito all'interno di ciascun sistema corporeo in ordine decrescente di frequenza:
Gastrointestinale: Diarrea, dispepsia, dolore addominale, costipazione, vomito
Neurologico: Vertigini, sonnolenza, ambliopia
Respiratorio: Reazione di ipersensibilità polmonare acuta (vedi AVVERTENZE )
Allergico: Prurito, orticaria
dermatologico: Alopecia
Varie: Febbre, brividi, malessere
I seguenti eventi avversi clinici aggiuntivi sono stati segnalati con l'uso di nitrofurantoina:
Gastrointestinale: Scialoadenite, pancreatite. Ci sono state segnalazioni sporadiche di colite pseudomembranosa con l'uso di nitrofurantoina. L'insorgenza di sintomi di colite pseudomembranosa può verificarsi durante o dopo il trattamento antimicrobico. (Vedere AVVERTENZE .)
Neurologico: Si è verificata una neuropatia periferica, che può diventare grave o irreversibile. Sono stati segnalati decessi. Condizioni come insufficienza renale (clearance della creatinina inferiore a 60 ml al minuto o creatinina sierica elevata clinicamente significativa), anemia, diabete mellito, squilibrio elettrolitico, carenza di vitamina B e malattie debilitanti possono aumentare la possibilità di neuropatia periferica. (Vedere AVVERTENZE .)
Sono stati segnalati anche astenia, vertigini e nistagmo con l'uso di nitrofurantoina.
Raramente sono stati riportati ipertensione endocranica benigna (pseudotumor cerebri), confusione, depressione, neurite ottica e reazioni psicotiche. Raramente sono state riportate fontanelle sporgenti, come segno di ipertensione endocranica benigna nei bambini.
Respiratorio
CON L'USO DI NITROFURANTOINA POSSONO AVERE REAZIONI DI IPERSENSIBILITA' POLMONARE CRONICA, SUBACUTE O ACUTA.
LE REAZIONI POLMONARI CRONICHE SI VERIFICANO IN GENERALE IN PAZIENTI CHE HANNO RICEVUTO TRATTAMENTO CONTINUO PER SEI MESI O PIÙ LUNGO. MALESI, DISPNEA DA SFORZO, TOSSE E FUNZIONALITÀ POLMONARE ALTERATA SONO MANIFESTAZIONI COMUNI CHE POSSONO AVERE INSIDIOSAMENTE. I RISULTATI RADIOLOGICI E ISTOLOGICI DI PNEUMONITE INTERSTIZIALE DIFFUSA O FIBROSI, O ENTRAMBI, SONO ANCHE MANIFESTAZIONI COMUNI DELLA REAZIONE POLMONARE CRONICA. LA FEBBRE È RARAMENTE IMPORTANTE
LA GRAVITÀ DELLE REAZIONI POLMONARI CRONICHE E IL LORO GRADO DI RISOLUZIONE SEMBRA ESSERE CORRELATA ALLA DURATA DELLA TERAPIA DOPO LA COMPARSA DEI PRIMI SEGNI CLINICI. LA FUNZIONE POLMONARE PUÒ ESSERE DANNEGGIATA PERMANENTEMENTE, ANCHE DOPO LA CESSAZIONE DELLA TERAPIA. IL RISCHIO È MAGGIORE QUANDO LE REAZIONI POLMONARI CRONICHE NON VENGONO RICONOSCIUTE PRECOCEMENTE.
Nelle reazioni polmonari subacute, febbre ed eosinofilia si verificano meno frequentemente rispetto alla forma acuta. Al termine della terapia, il recupero può richiedere diversi mesi. Se i sintomi non vengono riconosciuti come correlati al farmaco e la terapia con nitrofurantoina non viene interrotta, i sintomi possono diventare più gravi.
Le reazioni polmonari acute si manifestano comunemente con febbre, brividi, tosse, dolore toracico, dispnea, infiltrazione polmonare con consolidamento o versamento pleurico ai raggi X ed eosinofilia. Le reazioni acute di solito si verificano entro la prima settimana di trattamento e sono reversibili con l'interruzione della terapia. La risoluzione spesso è drammatica. (Vedere AVVERTENZE .)
Sono state riportate variazioni dell'ECG (p. es., variazioni dell'onda ST/T non specifiche, blocco di branca) in associazione con reazioni polmonari.
La cianosi è stata segnalata raramente.
epatico: Raramente si verificano reazioni epatiche, tra cui epatite, ittero colestatico, epatite cronica attiva e necrosi epatica. (Vedere AVVERTENZE .)
Allergico: È stata segnalata la sindrome simil-lupus associata a reazione polmonare alla nitrofurantoina. Inoltre, angioedema; eruzioni maculopapulari, eritematose o eczematose; anafilassi; artralgia; mialgia; febbre da droga; brividi; e sono state riportate vasculite (talvolta associata a reazioni polmonari). Le reazioni di ipersensibilità rappresentano gli eventi avversi segnalati spontaneamente più frequenti nell'esperienza post-marketing mondiale con le formulazioni di nitrofurantoina.
dermatologico: Raramente sono stati segnalati dermatite esfoliativa ed eritema multiforme (compresa la sindrome di Stevens-Johnson).
Ematologico: Raramente è stata segnalata cianosi secondaria a metaemoglobinemia.
Varie: Come con altri agenti antimicrobici, possono verificarsi superinfezioni causate da organismi resistenti, ad es. specie Pseudomonas o specie Candida.
Negli studi clinici su Macrobid, gli eventi avversi di laboratorio più frequenti (1-5%), indipendentemente dalla relazione farmacologica, sono stati i seguenti: eosinofilia, aumento di AST (SGOT), aumento di ALT (SGPT), diminuzione dell'emoglobina, aumento del fosforo sierico. Con l'uso della nitrofurantoina sono stati segnalati anche i seguenti eventi avversi di laboratorio: anemia da deficit di glucosio-6-fosfato deidrogenasi (vedere AVVERTENZE ), agranulocitosi, leucopenia, granulocitopenia, anemia emolitica, trombocitopenia, anemia megaloblastica. Nella maggior parte dei casi, queste anomalie ematologiche si sono risolte dopo l'interruzione della terapia. Raramente è stata segnalata anemia aplastica.
INTERAZIONI DI DROGA
Gli antiacidi contenenti trisilicato di magnesio, quando somministrati in concomitanza con nitrofurantoina, riducono sia la velocità che l'entità dell'assorbimento. Il meccanismo di questa interazione è probabilmente l'adsorbimento della nitrofurantoina sulla superficie del trisilicato di magnesio.
I farmaci uricosurici, come il probenecid e il sulfinpirazone, possono inibire la secrezione tubulare renale di nitrofurantoina. Il conseguente aumento dei livelli sierici di nitrofurantoina può aumentare la tossicità e la diminuzione dei livelli urinari potrebbe ridurne l'efficacia come antibatterico delle vie urinarie.

Interazioni farmacologiche/test di laboratorio
A causa della presenza di nitrofurantoina, può verificarsi una reazione falsa positiva per il glucosio nelle urine. Questo è stato osservato con le soluzioni di Benedict e Fehling ma non con il test enzimatico del glucosio.
AVVERTENZE
Reazioni polmonari
REAZIONI POLMONARI ACUTE, SUBACUTE O CRONICHE SONO STATI OSSERVATE IN PAZIENTI TRATTATI CON NITROFURANTOINA. SE SI VERIFICANO QUESTE REAZIONI, MACROBID 100mg DEVE ESSERE INTERROTTO E PRENDERE APPROPRIATE MISURE. I RAPPORTI HANNO CITATO REAZIONI POLMONARI COME CAUSA CONTRIBUENTE DI MORTE.
LE REAZIONI POLMONARI CRONICHE (POLMONITE INTERSTIZIALE DIFFUSA O FIBROSI POLMONARE, O ENTRAMBI) POSSONO SVILUPPARSI INSIDIOSAMENTE. QUESTE REAZIONI SI VERIFICANO RARAMENTE E IN GENERE IN PAZIENTI CHE FANNO TERAPIA PER SEI MESI O PIÙ LUNGO. VIENE GARANTITO UN RAVVICINATO MONITORAGGIO DELLA CONDIZIONE POLMONARE DEI PAZIENTI CHE RICEVONO TERAPIA A LUNGO TERMINE E RICHIEDE CHE I BENEFICI DELLA TERAPIA SIANO VALUTATI CONTRO I POTENZIALI RISCHI. (VEDERE REAZIONI RESPIRATORIE .)
Epatotossicità
Raramente si verificano reazioni epatiche, tra cui epatite, ittero colestatico, epatite cronica attiva e necrosi epatica. Sono stati segnalati decessi. L'esordio dell'epatite cronica attiva può essere insidioso e i pazienti devono essere monitorati periodicamente per eventuali cambiamenti nei test biochimici che indicherebbero un danno epatico. Se si verifica epatite, il farmaco deve essere sospeso immediatamente e devono essere prese le misure appropriate.
Neuropatia
Si è verificata una neuropatia periferica, che può diventare grave o irreversibile. Sono stati segnalati decessi. Condizioni come insufficienza renale (clearance della creatinina inferiore a 60 ml al minuto o creatinina sierica elevata clinicamente significativa), anemia, diabete mellito, squilibrio elettrolitico, carenza di vitamina B e malattie debilitanti possono aumentare l'insorgenza di neuropatia periferica. I pazienti che ricevono una terapia a lungo termine devono essere monitorati periodicamente per rilevare eventuali alterazioni della funzione renale. La neurite ottica è stata segnalata raramente nell'esperienza post-marketing con le formulazioni di nitrofurantoina.
Anemia emolitica
Casi di anemia emolitica del tipo a sensibilità alla primachina sono stati indotti dalla nitrofurantoina. L'emolisi sembra essere collegata a un deficit di glucosio-6-fosfato deidrogenasi nei globuli rossi dei pazienti affetti. Questa carenza si riscontra nel 10 per cento dei neri e in una piccola percentuale di gruppi etnici di origine mediterranea e del Vicino Oriente. L'emolisi è un'indicazione per interrompere Macrobid; l'emolisi cessa quando il farmaco viene sospeso.
Diarrea associata a Clostridium difficile
La diarrea associata al Clostridium difficile (CDAD) è stata segnalata con l'uso di quasi tutti gli agenti antibatterici, inclusa la nitrofurantoina, e può variare in gravità da diarrea lieve a colite fatale. Il trattamento con agenti antibatterici altera la normale flora del colon portando alla crescita eccessiva di C. difficile.
C. difficile produce le tossine A e B che contribuiscono allo sviluppo del CDAD. I ceppi produttori di ipertossine di C. difficile causano un aumento della morbilità e della mortalità, poiché queste infezioni possono essere refrattarie alla terapia antimicrobica e possono richiedere una colectomia. La CDAD deve essere considerata in tutti i pazienti che presentano diarrea in seguito all'uso di antibiotici. È necessaria un'attenta anamnesi poiché è stato segnalato che CDAD si verifica più di due mesi dopo la somministrazione di agenti antibatterici.
Se si sospetta o si conferma la CDAD, potrebbe essere necessario interrompere l'uso continuo di antibiotici non diretti contro C. difficile. Come clinicamente indicato, devono essere istituiti un'appropriata gestione dei fluidi e degli elettroliti, l'integrazione proteica, il trattamento antibiotico del C. difficile e la valutazione chirurgica.
PRECAUZIONI
Generale
È improbabile che la prescrizione di Macrobid 50 mg in assenza di un'infezione batterica provata o fortemente sospetta o di un'indicazione profilattica fornisca benefici al paziente e aumenti il rischio di sviluppo di batteri resistenti ai farmaci.
Cancerogenesi, mutagenesi, compromissione della fertilità
La nitrofurantoina non è risultata cancerogena quando somministrata a ratti Holtzman femmine per 44,5 settimane o a ratti Sprague-Dawley femmine per 75 settimane. Due saggi biologici per roditori cronici che utilizzano ratti Sprague-Dawley maschi e femmine e due saggi biologici cronici in topi svizzeri e in topi BDF1 non hanno rivelato alcuna evidenza di cancerogenicità.
La nitrofurantoina ha presentato prove di attività cancerogena nei topi B6C3F1 femmine, come dimostrato dall'aumentata incidenza di adenomi tubulari, tumori misti benigni e tumori delle cellule della granulosa dell'ovaio. Nei ratti maschi F344/N, si è verificata un'aumentata incidenza di neoplasie non comuni delle cellule tubulari renali, osteosarcomi dell'osso e neoplasie del tessuto sottocutaneo. In uno studio che prevedeva la somministrazione sottocutanea di 75 mg/kg di nitrofurantoina a femmine di topo gravide, nella generazione F1 sono stati osservati adenomi papillari polmonari di significato sconosciuto.
È stato dimostrato che la nitrofurantoina induce mutazioni puntiformi in alcuni ceppi di Salmonella typhimurium e mutazioni in avanti nelle cellule di linfoma murino L5178Y. La nitrofurantoina ha indotto un aumento del numero di scambi di cromatidi fratelli e aberrazioni cromosomiche nelle cellule dell'ovaio di criceto cinese ma non nelle cellule umane in coltura. I risultati del test letale recessivo legato al sesso nella Drosophila erano negativi dopo la somministrazione di nitrofurantoina mediante alimentazione o iniezione. La nitrofurantoina non ha indotto mutazioni ereditarie nei modelli di roditori esaminati.
Il significato dei risultati di cancerogenicità e mutagenicità relativi all'uso terapeutico della nitrofurantoina nell'uomo è sconosciuto.
La somministrazione di alte dosi di nitrofurantoina ai ratti provoca un temporaneo arresto spermatogeno; questo è reversibile con l'interruzione del farmaco. Dosi di 10 mg/kg/die o superiori in maschi umani sani possono, in alcuni casi imprevedibili, produrre un arresto spermatogeno da lieve a moderato con una diminuzione del numero di spermatozoi.
Gravidanza
Effetti teratogeni - Gravidanza Categoria B
Diversi studi sulla riproduzione sono stati condotti su conigli e ratti a dosi fino a sei volte la dose umana e non hanno rivelato prove di ridotta fertilità o danni al feto dovuti alla nitrofurantoina. In un singolo studio pubblicato condotto su topi a 68 volte la dose umana (basata su mg/kg somministrati alla madre), sono stati osservati un ritardo della crescita e una bassa incidenza di malformazioni minori e comuni. Tuttavia, a 25 volte la dose umana, non sono state osservate malformazioni fetali; la rilevanza di questi risultati per l'uomo è incerta. Non ci sono, tuttavia, studi adeguati e ben controllati sulle donne in gravidanza. Poiché gli studi sulla riproduzione animale non sono sempre predittivi della risposta umana, questo farmaco deve essere usato durante la gravidanza solo se chiaramente necessario.
Effetti non teratogeni
In uno studio pubblicato sulla cancerogenicità transplacentare, la nitrofurantoina ha dimostrato di indurre adenomi papillari polmonari nei topi di generazione F1 a dosi 19 volte la dose umana su base mg/kg. La relazione di questa scoperta con la potenziale cancerogenesi umana è attualmente sconosciuta. A causa dell'incertezza sulle implicazioni umane di questi dati sugli animali, questo farmaco dovrebbe essere usato durante la gravidanza solo se chiaramente necessario.
Lavoro e consegna
Vedere CONTROINDICAZIONI .
Madri che allattano
La nitrofurantoina è stata rilevata nel latte materno umano in tracce. A causa delle potenziali reazioni avverse gravi dovute alla nitrofurantoina nei lattanti di età inferiore a un mese, si deve decidere se interrompere l'allattamento o interrompere il farmaco, tenendo conto dell'importanza del farmaco per la madre. (Vedere CONTROINDICAZIONI .)
Uso pediatrico
Macrobid 100 mg sono controindicati nei bambini di età inferiore a un mese. (Vedere CONTROINDICAZIONI .) La sicurezza e l'efficacia nei pazienti pediatrici di età inferiore ai dodici anni non sono state stabilite.
Uso geriatrico
Gli studi clinici su Macrobid 50 mg non hanno incluso un numero sufficiente di soggetti di età pari o superiore a 65 anni per determinare se rispondono in modo diverso dai soggetti più giovani. Altre esperienze cliniche riportate non hanno identificato differenze nelle risposte tra i pazienti anziani e quelli più giovani. Rapporti spontanei suggeriscono una percentuale maggiore di reazioni polmonari, inclusi i decessi, nei pazienti anziani; queste differenze sembrano essere correlate alla percentuale più alta di pazienti anziani che ricevono una terapia a lungo termine con nitrofurantoina. Come nei pazienti più giovani, le reazioni polmonari croniche si osservano generalmente nei pazienti che ricevono la terapia per sei mesi o più (vedi AVVERTENZE ). Segnalazioni spontanee suggeriscono anche un aumento della proporzione di reazioni epatiche gravi, inclusi i decessi, nei pazienti anziani (vedi AVVERTENZE ).
In generale, quando si prescrive Macrobid deve essere presa in considerazione la maggiore frequenza di ridotta funzionalità epatica, renale o cardiaca e di malattie concomitanti o altre terapie farmacologiche nei pazienti anziani. Questo farmaco è noto per essere sostanzialmente escreto dai reni e il rischio di reazioni tossiche a questo farmaco può essere maggiore nei pazienti con funzionalità renale compromessa. Anuria, oliguria o compromissione significativa della funzione renale (clearance della creatinina inferiore a 60 ml al minuto o creatinina sierica elevata clinicamente significativa) sono controindicazioni (vedi CONTROINDICAZIONI ). Poiché è più probabile che i pazienti anziani presentino una ridotta funzionalità renale, può essere utile monitorare la funzionalità renale.
OVERDOSE
Occasionali episodi di sovradosaggio acuto di nitrofurantoina non hanno provocato sintomi specifici diversi dal vomito. Si raccomanda l'induzione del vomito. Non esiste un antidoto specifico, ma deve essere mantenuta un'elevata assunzione di liquidi per favorire l'escrezione urinaria del farmaco. La nitrofurantoina è dializzabile.
CONTROINDICAZIONI
Anuria, oliguria o compromissione significativa della funzione renale (clearance della creatinina inferiore a 60 ml al minuto o creatinina sierica elevata clinicamente significativa) sono controindicazioni. Il trattamento di questo tipo di pazienti comporta un aumentato rischio di tossicità a causa della ridotta escrezione del farmaco.
A causa della possibilità di anemia emolitica dovuta a sistemi enzimatici eritrocitari immaturi (instabilità del glutatione), il farmaco è controindicato nelle pazienti in gravidanza a termine (38-42 settimane di gestazione), durante il travaglio e il parto o quando l'inizio del travaglio è imminente. Per lo stesso motivo, il farmaco è controindicato nei neonati di età inferiore a un mese.
Macrobid 50 mg è controindicato nei pazienti con una precedente storia di ittero colestatico/disfunzione epatica associata a nitrofurantoina.
Macrobid 100 mg è anche controindicato in quei pazienti con nota ipersensibilità alla nitrofurantoina.
FARMACOLOGIA CLINICA
Ogni capsula di Macrobid da 100 mg contiene due forme di nitrofurantoina. Il 25% è costituito da nitrofurantoina macrocristallina, che ha una dissoluzione e un assorbimento più lenti rispetto alla nitrofurantoina monoidrato. Il restante 75% è nitrofurantoina monoidrato contenuta in una miscela di polvere che, per esposizione ai liquidi gastrici e intestinali, forma una matrice gel che rilascia nitrofurantoina nel tempo. Sulla base dei dati di farmacocinetica urinaria, l'entità e la velocità di escrezione urinaria di nitrofurantoina dalla capsula di Macrobid da 100 mg sono simili a quelle della capsula di Macrodantin® (macrocristalli di nitrofurantoina) da 50 mg o 100 mg. Circa il 20-25% di una singola dose di nitrofurantoina viene recuperato dalle urine immodificato nelle 24 ore.
Le concentrazioni plasmatiche di nitrofurantoina dopo una singola dose orale della capsula di Macrobid da 100 mg sono basse, con livelli di picco generalmente inferiori a 1 mcg/mL. La nitrofurantoina è altamente solubile nelle urine, alle quali può conferire un colore marrone. Quando Macrobid viene somministrato con il cibo, la biodisponibilità della nitrofurantoina aumenta di circa il 40%.
Microbiologia
La nitrofurantoina è un agente antimicrobico nitrofurano con attività contro alcuni batteri Gram-positivi e Gram-negativi.
Meccanismo di azione
Il meccanismo dell'azione antimicrobica della nitrofurantoina è insolito tra gli antibatterici. La nitrofurantoina è ridotta dalle flavoproteine batteriche a intermedi reattivi che inattivano o alterano le proteine ribosomiali batteriche e altre macromolecole. Come risultato di tali inattivazioni, i processi biochimici vitali della sintesi proteica, del metabolismo energetico aerobico, della sintesi del DNA, della sintesi dell'RNA e della sintesi della parete cellulare sono inibiti. La nitrofurantoina è battericida nelle urine a dosi terapeutiche. La natura ampia di questa modalità d'azione può spiegare la mancanza di resistenza batterica acquisita alla nitrofurantoina, poiché le necessarie mutazioni multiple e simultanee delle macromolecole bersaglio sarebbero probabilmente letali per i batteri.
Interazioni con altri antibiotici
L'antagonismo è stato dimostrato in vitro tra nitrofurantoina e antimicrobici chinolonici. Il significato clinico di questo risultato è sconosciuto.
Sviluppo della Resistenza
Lo sviluppo della resistenza alla nitrofurantoina non è stato un problema significativo dalla sua introduzione nel 1953. Non è stata osservata resistenza crociata con antibiotici e sulfamidici e la resistenza trasferibile è, al massimo, un fenomeno molto raro.
La nitrofurantoina ha dimostrato di essere attiva contro la maggior parte dei ceppi dei seguenti batteri sia in vitro che nelle infezioni cliniche [vedi INDICAZIONI E UTILIZZO ):
Microrganismi Gram-positivi aerobici e facoltativi
Staphylococcus saprophyticus
Microrganismi Gram-negativi aerobici e facoltativi
Escherichia coli
Almeno il 90 percento dei seguenti microrganismi mostra una concentrazione inibitoria minima (MIC) in vitro inferiore o uguale al punto di rottura suscettibile per la nitrofurantoina. Tuttavia, l'efficacia della nitrofurantoina nel trattamento delle infezioni cliniche dovute a questi microrganismi non è stata stabilita in studi adeguati e ben controllati.
Microrganismi Gram-positivi aerobici e facoltativi
Stafilococchi coagulasi negativi (incluso Staphylococcus epidermidis) Enterococcus faecalis Staphylococcus aureus Streptococcus aga/actiae
Streptococchi di gruppo 0
Streptococchi del gruppo Viridans
Microrganismi Gram-negativi aerobici e facoltativi:
Citrobacter ama/onaticus Citrobacter diversus Citrobacter freundii Klebsiella oxytoca Klebsiella ozaenae
La nitrofurantoina non è attiva contro la maggior parte dei ceppi delle specie Proteus o Serratia. Non ha attività contro le specie Pseudomonas.
Metodi di prova di sensibilità
Quando disponibile, il laboratorio di microbiologia clinica deve fornire al medico i risultati cumulativi dei test di sensibilità in vitro per i farmaci antimicrobici utilizzati negli ospedali residenti sotto forma di rapporti periodici che descrivono il profilo di suscettibilità dei patogeni nosocomiali e acquisiti in comunità. Questi rapporti dovrebbero aiutare il medico nella scelta dell'antimicrobico più efficace.
Tecniche di diluizione: metodi quantitativi vengono utilizzati per determinare le concentrazioni minime inibitorie antimicrobiche (MIC). Questi MIC forniscono stime della suscettibilità dei batteri ai composti antimicrobici. I MIC dovrebbero essere determinati utilizzando una procedura standardizzata. Le procedure standardizzate si basano su un metodo di diluizione (brodo o agar) (1) o equivalente con concentrazioni standardizzate di inoculo e concentrazioni standardizzate di nitrofurantoina in polvere. I valori MIC devono essere interpretati secondo i criteri forniti nella Tabella 1.
Tecnica di diffusione: metodi quantitativi che richiedono la misurazione dei diametri delle zone forniscono anche stime riproducibili della suscettibilità dei batteri ai composti antimicrobici. Una di queste procedure standardizzate (2) richiede l'uso di concentrazioni standardizzate di inoculo. Questa procedura utilizza dischi di carta impregnati con 300 pg di nitrofurantoina per testare la suscettibilità dei microrganismi alla nitrofurantoina. I criteri interpretativi della diffusione del disco sono forniti nella Tabella 1.
Un rapporto di Suscettibile indica che è probabile che l'agente patogeno venga inibito se il composto antimicrobico nelle urine raggiunge le concentrazioni normalmente ottenibili. Un rapporto di Intermedio indica che il risultato deve essere considerato equivoco e, se il microrganismo non è completamente suscettibile a farmaci alternativi clinicamente fattibili, il test deve essere ripetuto. Questa categoria implica una possibile applicabilità clinica in sedi corporee in cui il farmaco è fisiologicamente concentrato o in situazioni in cui può essere utilizzato un dosaggio elevato di farmaco. Questa categoria fornisce anche una zona cuscinetto, che impedisce a piccoli fattori tecnici incontrollati di causare grandi discrepanze nell'interpretazione. Un report di Resistance indica che è improbabile che il patogeno venga inibito se il composto antimicrobico nelle urine raggiunge le concentrazioni normalmente ottenibili; dovrebbe essere selezionata un'altra terapia.
Controllo di qualità: Le procedure di prova di sensibilità standardizzate richiedono l'uso di microrganismi di controllo della qualità per controllare gli aspetti tecnici delle procedure di prova (3). La polvere di nitrofurantoina standard dovrebbe fornire il seguente intervallo di valori indicati nella tabella 2.
Studi clinici
Studi clinici controllati che hanno confrontato Macrobid 100 mg PO ogni 12 ore e Macrodantin 50 mg PO ogni 6 ore nel trattamento delle infezioni acute del tratto urinario non complicate hanno dimostrato un'eradicazione microbiologica di circa il 75% dei patogeni sensibili in ciascun gruppo di trattamento.
INFORMAZIONI PER IL PAZIENTE
I pazienti devono essere avvisati di assumere Macrobid 100 mg con il cibo (idealmente colazione e cena) per aumentare ulteriormente la tolleranza e migliorare l'assorbimento del farmaco. I pazienti devono essere istruiti a completare l'intero ciclo di terapia; tuttavia, si dovrebbe consigliare loro di contattare il proprio medico se si verificano sintomi insoliti durante la terapia.
I pazienti devono essere avvisati di non usare preparati antiacidi contenenti trisilicato di magnesio durante l'assunzione di Macrobid.
pazienti devono essere informati che i farmaci antibatterici, incluso Macrobid, devono essere usati solo per trattare le infezioni batteriche. Non trattano le infezioni virali (p. es., il comune raffreddore). Quando Macrobid 100 mg viene prescritto per il trattamento di un'infezione batterica, i pazienti devono essere informati che, sebbene sia comune sentirsi meglio all'inizio della terapia, il farmaco deve essere assunto esattamente come indicato. Saltare le dosi o non completare l'intero ciclo di terapia può (1) diminuire l'efficacia del trattamento immediato e (2) aumentare la probabilità che i batteri sviluppino resistenza e non siano curabili con Macrobid o altri farmaci antibatterici in futuro.
La diarrea è un problema comune causato dagli antibiotici che di solito termina quando l'antibiotico viene interrotto. A volte, dopo l'inizio del trattamento con antibiotici, i pazienti possono sviluppare feci acquose e sanguinolente (con o senza crampi allo stomaco e febbre) anche fino a due o più mesi dopo aver assunto l'ultima dose di antibiotico. Se ciò si verifica, i pazienti devono contattare il proprio medico il prima possibile.
